
色谱课堂
动态载量高
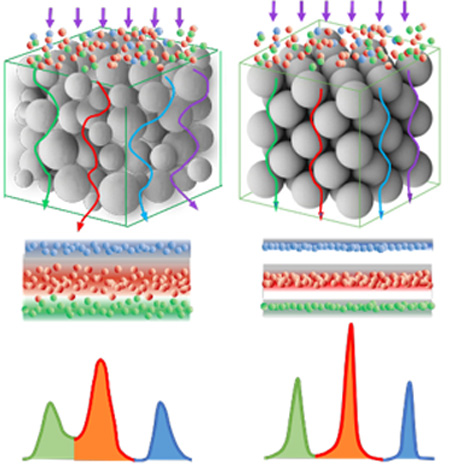
单分散色谱填料动态吸附穿透曲线更陡峭,在相同的穿透比例时,达到的吸附载量更高;
洗脱更集中
单分散色谱填料的洗脱峰更高更窄,分离度更好,洗脱更集中,样品浓度更高,洗脱体积更小,后续浓缩等生产效率更高;
纯化效果好
在产品质量要求(纯度,收率)相同的情况下,可以提高进样量,增加工艺载量提高工艺效率,或者在工艺载量和收率不变的情况下,获得纯度更高的产品;
反压更低,效率更高
单分散色谱填料不容易堵塞筛板,并可以使用更大孔径的筛板,因此系统压力低、流速快、重复性好,有利于提高生产效率;
填料使用寿命更长
单分散填料表面受力分散均匀,不易破碎,有更长的使用寿命;
批次重复性好
单分散色谱填料装填的色谱柱柱床稳定,重复性好。
联系我们
纳微印度公司
Suzhou Nanomicro Tech India Private Limited
Address: 1033, Tower A, Ithum Building, plot-A40 Noida Sector 62, Gsutam Buddha Nagar Uttar Pradesh 201301, INDIA
Phone: +91 96548 80558
纳微美国公司
Nanomicro Technologies Inc.
Address:196 E Main Street #210, Milford, MA 01757
Phone: +1-(508) 338-3051
Copyright © 2019 苏州纳微 All rights reserved
Email:info@nanomicrotech.com 苏ICP备15038436号-1 网站建设:中企动力 苏州


















 中小分子
中小分子